
lavanguardia.com
Antes de dar el “sí” definitivo a su doctora, Cecilia Rodríguez había pasado por quimioterapia, radioterapia e inmunoterapia. El cáncer con el que convive desde hace seis años se había extendido y la oncóloga le habló del tratamiento experimental que estaba probando una farmacéutica japonesa en Barcelona. Así comenzó su primera experiencia como paciente en un ensayo clínico para intentar reducir la carga tumoral de la metástasis. Por ahora, no ha crecido más. Aunque no sabe si la medicación terminará funcionando, Cecilia asegura que su calidad de vida ha mejorado y que, en los últimos seis meses siendo parte de esta investigación, ya ha notado un “alivio emocional impresionante”.
Algo parecido le sucedió a Maria Masferrer (nombre ficticio) cuando le propusieron sumarse a un ensayo, también en la capital catalana, para probar una cura que erradique la enfermedad crónica que arrastra desde hace tiempo. “Es una vacuna experimental. Cuando no tienes otra opción o las que hay no son satisfactorias, no tienes nada que perder”, relata. Los próximos meses, seguirá bajo un control estricto por parte de sus médicos para comprobar la eficacia del tratamiento: “Los riesgos son mínimos y al final también es una contribución desinteresada a la ciencia por mi parte”.
lavanguardia.com
lavanguardia.com
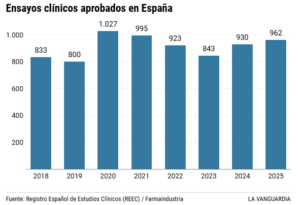
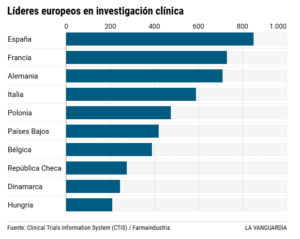
Tanto Cecilia como Maria son una parte esencial del engranaje de la investigación clínica, una carrera de fondo en la que España ha tomado la delantera en los últimos años dentro del continente europeo. Sólo el año pasado, la inversión en I+D en España de la industria farmacéutica se acercó a los 1.700 millones de euros. Y la mayor parte fue a los ensayos clínicos. Un estudio de Farmaindustria elaborado con datos del Registro Español de Estudios Clínicos (REEC) constata que el año pasado se autorizaron 962 ensayos clínicos con medicamentos en territorio español. Esta cifra récord situa al país como líder europeo con mayor número de investigaciones, por delante de Francia, Alemania o Italia. Cuatro de cada diez estudios se dedicaron a buscar nuevos fármacos contra el cáncer, la patología más tratada seguida por las del sistema inmunitario, el nervioso y el cardiovascular. La asociación calcula que cerca de 170.000 pacientes españoles están participando actualmente en algún tipo de ensayo. El potencial económico de esta actividad es evidente.
Pero el liderazgo -explica la directora de Investigación Clínica y Traslacional de Farmaindustria, Amelia Martín Uranga- no ha surgido de la noche a la mañana. “Fuimos el primer país en implementar el reglamento europeo de ensayos clínicos. Esa regulación pionera fue clave”, afirma. A este impulso temprano de la normativa se le suman otros factores, como una red hospitalaria con casi 1.000 centros implicados en ensayos clínicos en los últimos cinco años, un perfil de paciente “altruista” -España tiene una de las mejores tasas de reclutamiento- y un modelo de colaboración público-privada en el que las compañías farmacéuticas financian más del 80% de estos estudios.
Un ensayo clínico es una investigación experimental que se hace en humanos -pueden estar sanos o enfermos- para evaluar la eficacia y seguridad de nuevos medicamentos o técnicas diagnósticas. Son indispensables para el avance de la medicina y los tienen que aprobar los comités de ética y autoridades sanitarias pertinentes.
El año pasado se autorizaron 962 ensayos clínicos con medicamentos en territorio español
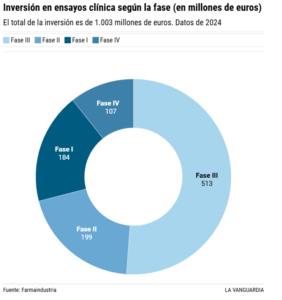
Estos estudios se dividen en fases que avanzan progresivamente hasta que los medicamentos consiguen llegar al mercado. La primera y más inicial se hace con grupos pequeños de menos de 100 personas para evaluar la seguridad del fármaco. La segunda amplia el número de pacientes hasta el millar para medir la eficacia. La tercera se usa para confirmar la seguridad y eficacia, ajustar la dosis óptima y medir los posibles efectos secundarios. En este punto ya hablamos de poblaciones mucho más grandes de miles de personas y se cuenta con la participación de hospitales de distintos continentes para comparar perfiles genéticos. Por último, la cuarta fase es de seguimiento una vez ya se ha comercializado el fármaco.
España cuenta con el hospital que lidera más investigaciones clínicas de toda Europa. El campus de Vall d’Hebron de Barcelona —que incluye el Vall Hebron Institut de Recerca (VHIR) y el Vall Hebron Institut d’Oncologia (VHIO)— albergó más de 2.200 estudios abiertos a lo largo de 2025, de los cuales más de 1.800 fueron ensayos clínicos, explica el doctor Xavier Cañas, director de Investigación Clínica Comercial y Contratada del VHIR. La mitad se centraron solo en los campos de la oncología y la hematología. “Durante 2025 hemos gestionado más de 2.300 pacientes, 2.300 esperanzas que esperan mejorar su salud”, remarca.
Como recuerda el doctor Josep Comín, director de Innovación, Investigación y Universidades de la Gerencia del Hospital de Bellvitge-Viladecans, los ensayos clínicos forman parte de la “misión” de los hospitales. “Mejoran la calidad asistencial de los pacientes, nos ayudan a estandarizar muchos procesos y dan acceso a innovaciones terapéuticas de último minuto”, remarca. En este centro han profesionalizado una unidad que lleva 270 investigaciones en activo, cuenta con 161 promotores distintos y está testeando en un millar de pacientes.
Lavanguardia.com
En el otro extremo de esta cadena por la que circula la innovación están las compañías farmacéuticas. La gran mayoría de las que escogen España para probar sus medicamentos son corporaciones extranjeras, y estas también han ido echando raíces con más centros de I+D y hubs de salud digital. La directora de Operaciones Clínicas de la estadounidense Bristol Myers Squibb (BMS) para España y Portugal, Yolanda Martínez, recuerda que ya es el segundo país para la compañía después de EE.UU., tanto en número de ensayos como de pacientes incluidos.
“Estamos transicionando de ser un país muy buen reclutador de pacientes a generar cada vez más evidencia clínica”, destaca sobre el creciente porcentaje de ensayos en fases tempranas (1 y 2), en las cuales los investigadores locales pueden tener un papel mucho más activo en las etapas iniciales del desarrollo de los fármacos. El grupo cuenta con un centro de investigación translacional en Sevilla que se dedica a convertir los descubrimientos del laboratorio en aplicaciones reales para los pacientes.
El 80% de estos estudios los financia la industria farmacéutica a través de hospitales y centros de I+D
Otro de los gigantes del sector, la suiza Roche, destinó 57,1 millones de euros a investigación clínica en España en 2025, una inversión que le permitió impulsar 283 ensayos clínicos sobre 76 moléculas diferentes. En estos ensayos participaron más de 8.500 pacientes -en esta métrica solo está por detrás de Estados Unidos y China- y cerca de un millar de profesionales sanitarios de 178 hospitales. “La inmensa mayoría de los medicamentos de Roche que hoy reciben los pacientes de todo el mundo en áreas como oncohematología, neurología u oftalmología, han pasado por España en algún momento en su fase de investigación y desarrollo”, responde vía correo electrónico Mariluz Amador, directora del departamento médico de Roche Farma España.
Por otro lado, la también helvética Novartis impulsó 255 ensayos clínicos en España durante el año pasado, con la colaboración de más de 150 centros investigadores, 2.850 profesionales y la participación de 7.140 pacientes. “En este impulso a la innovación, ponemos el foco en grandes retos de la salud como el cáncer y las enfermedades cardiovasculares, las dos principales causas de muerte en España”, cuentan des de la multinacional farmacéutica.
Aún así, tanto la industria farmacéutica como los centros sanitarios comparten algunos de los principales retos a los que se enfrenta España para conseguir mejorar esta posición, sobre todo ante la pujante competencia de Estados Unidos y algunos países de la región Asia-Pacífico como China. “Hay que dar más facilidades regulatorias para que Europa siga siendo atractiva. Está bien tener en mente que existe la variable del coste económico, pero nosotros tenemos que jugar la carta del prestigio histórico para mantener España y Catalunya como centros de referencia”, indica Pau Alcubilla, facultativo de ensayos clínicos en el Hospital Clínic de Barcelona.

lavanguardia.com
Precisamente, Bristol Myers Squibb (BMS), la Asociación Española de Investigación sobre el Cáncer (ASEICA) y la Plataforma de Organizaciones de Pacientes (POP) presentaron a finales de febrero un informe en el cual alertaban que España podría dejar escapar el impacto que suponen los ensayos clínicos —estimaban un acumulado de 1.262 millones de euros hasta 2040— si no refuerza su papel innovador en este campo. Yolanda Martínez, de BMS, recuerda que aún persiste una brecha en el acceso a estos medicamentos de última generación en España, ya que, pese a haberse reducido, la espera hasta que llegan al mercado supera los 600 días.
Para Amelia Martín Uranga, de Farmaindustria, la coordinación entre agencias, comités éticos y hospitales ha sido clave para llegar hasta el punto actual, pero es necesario continuar reduciendo la burocracia que envuelve estos procesos. “La futura ley europea de biotecnología será muy importante porque viene a simplificar y a hacer más ágil la gestión de contratos entre el centro y el promotor”, incide. Xavier Cañas, de Vall Hebron, también defiende que es “crucial” reducir estos plazos: “Nosotros haremos nuestro trabajo con el mismo rigor, pero la toma de decisiones de una farmacéutica será distinta si en Europa tardamos más”. Bruselas se ha puesto las pilas y también ha lanzado el proyecto FAST-EU para acelerar la evaluación de ensayos clínicos de multinacionales en la UE.
Cerca de 170.000 pacientes españoles participan en una de estas pruebas, según Farmaindustria
Sobre la dependencia de las corporaciones estranjeras para sacar adelante estos ensayos, Josep Comín del Hospital de Bellvitge-Viladecas, recuerda que una de las asignaturas pendientes es reforzar la conexión con pequeñas startups autóctonas que quieran validar sus moléculas en las fases más tempranas de todo este ciclo.
Desde el sector coinciden en qué la digitalización, la inteligencia artificial y el uso de los datos marcarán el compás de las próximas décadas. El campo de la investigación clínica, añade Mariluz Amador de Roche, también avanza cada vez más rápido hacia la medicina personalizada: “Tenemos en el horizonte un modelo de sanidad más proactivo y eficiente, donde el diagnóstico de precisión y el perfil molecular permitan tratar cada enfermedad de la forma más adecuada para cada paciente en el momento oportuno”. Además, otro de los objetivos será descentralizar los ensayos para acercarlos a los pacientes y que estos no tengan que desplazarse innecesariamente para participar en ellos.

